Wie ein delokalisiertes Proton die DNA-Synthese antreibt
- Neues aus der Fakultät 2026
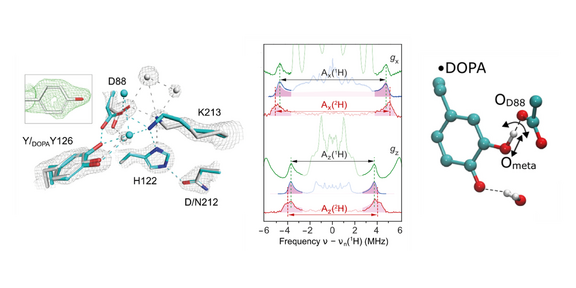
Die Forschenden zeigen, dass eine Wasserstoffbrückenbindung mit niedriger Barriere (low-barrier hydrogen bond, LBHB) mit einem delokalisierten Proton die katalytische Kraft für die weitreichende Radikalübertragung in metallfreien Ribonukleotid-Reduktasen (RNRs) bereitstellt. Diese LBHB moduliert den Redoxzustand des 3,4-Dihydroxyphenylalanin-Radikals (DOPA•) und ermöglicht so einen reversiblen Radikaltransport über große Distanzen im Enzym. Die Arbeit liefert damit erstmals direkte Belege für die Beteiligung von LBHBs in der Proteinchemie und unterstreicht die Bedeutung von Quanteneffekten in der Enzymkatalyse.
Um die molekularen Mechanismen aufzuklären, kombinierte das internationale Forschungsteam eine Reihe moderner Methoden, darunter EPR- und ENDOR-Spektroskopie, quantenchemische Berechnungen und Mutationsanalysen. Wichtige Beiträge zur experimentellen Charakterisierung des DOPA-Radikals lieferten Juliane John und Dr. Yury Kutin von der Technischen Universität Dortmund, die mithilfe hochauflösender ENDOR-Spektroskopie die Hyperfeinwechselwirkungen untersuchten und den LBHB-Zustand bestätigten.
Die Studie liefert erstmals detaillierte molekulare Einblicke in den Mechanismus der weitreichenden Radikalübertragung in RNRs und eröffnet neue Perspektiven für das Verständnis von Quanteneffekten in der Enzymkatalyse sowie für die Aufklärung der DNA-Synthese. Die internationale Studie wurde durch den Exzellenzcluster RESOLV (Ruhr Explores Solvation) unterstützt.
Publikation:
Low-barrier hydrogen bond powers long-range radical transfer in the metal-free ribonucleotide reductase
Abhishek Sirohiwal, Juliane John, Yury Kutin, Rohit Kumar, Federico Baserga, Vivek Srinivas, Hugo Lebrette,Maximilian C. Pöverlein, Ana P. Gamiz-Hernandez, Joachim Heberle, Müge Kasanmascheff, Martin Högbom, Ville R. I. Kaila
PNAS 2026, doi: 10.1073/pnas.2529856123






