Allosterische Modulation der Dynamik der Kinase p38alpha über die „Lipidbindende Domäne"
- Neues aus der Fakultät 2026
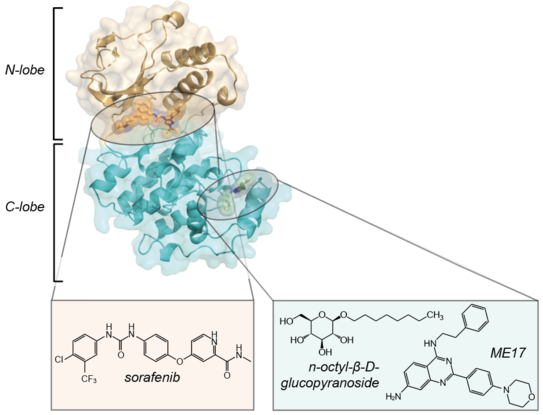
Proteinkinasen – Proteine, die Phosphatgruppen übertragen – sind die Hauptbestandteile zellulärer Signalkaskaden und überaus wichtige pharmakologische Targets, z. B. im Krebskontext. Leider ist die Architektur ihrer aktiven Taschen über die gesamte Familie der Kinasen konserviert. Entsprechend sind Inhibitoren, die darin binden sollen, meist unspezifisch und mit einer Vielzahl von Nebenwirkungen verknüpft. Allosterische Effektoren sind dagegen Moleküle, die an solche Regionen des Proteins binden, die keine direkte funktionale Bedeutung haben und trotz dessen einen pharmakologischen Effekt induzieren können. Während einer solchen Belegung manchmal direkte strukturelle Konsequenzen folgen, kann der allosterische Effekt auch rein über eine Modulation der Proteindynamik entstehen. Diese „dynamische Allosterie“ ist über herkömmliche Methoden der Strukturbiologie, insbesondere die Röntgenkristallographie oder die Cryo-Elektronenmikroskopie, schwer nachzuvollziehen.
Die Proteinkinase p38α besitzt in ihrem C-Lappen, genauer gesagt in der lipidbindenden Domäne, die sogenannte Lipidtasche, welche erst in Anwesenheit geeigneter Moleküle sichtbar wird (eine sogenannte kryptische Tasche). Obwohl verschiedene Moleküle, inkl. solcher, die typischen Medikamenten strukturell sehr ähnlich sind, nachweislich hier binden können, ist leider bislang noch kein modulierender Effekt bezüglich der Proteinfunktionalität beobachtet worden. Das wirft die grundlegende Frage auf, ob zwischen dieser Tasche und den aktiven Zentren der Kinase überhaupt eine allosterische Verbindung besteht oder nicht. In ihrer Arbeit zeigt Sara Medina Gomez aus dem Arbeitskreis Linser, dass das Binden verschiedener Liganden in die Lipidtasche trotz des Fehlens struktureller Folgen tatsächlich eine ganze Reihe von Konsequenzen nach sich zieht, die weiträumig das gesamte Protein überspannen. Mithilfe der NMR-Spektroskopie werden insbesondere Änderungen der chemischen Verschiebungen vieler Reste des Proteins beobachtet, die sich über die gesamte Architektur erstrecken, nicht nur lokal um die Lipidtasche herum, wie in Abwesenheit von allosterischen Interaktionen zu erwarten wäre. Zudem lässt sich anhand verschiedener Relaxationsparameter ersehen, dass die Proteindynamik insbesondere auf der „mittleren“ Zeitskala, im Mikrosekunden- bis Millisekundenbereich, durch die Liganden in der Lipidtasche beeinflusst wird. Wieder sind die Effekte nicht regional auf den C Lappen beschränkt, sondern erstrecken sich insbesondere auf funktionell wichtige Bereiche wie die Aktivierungsschleife und die aktive Tasche im N-Lappen. Die Bindung der Liganden in die Lipidtasche hat entsprechend eine globale Auswirkung auf das Konformationsensemble der insgesamt sehr plastischen Kinase und könnte damit potentiell universelle Veränderungen auch in der Funktionalität der Proteins hervorrufen.
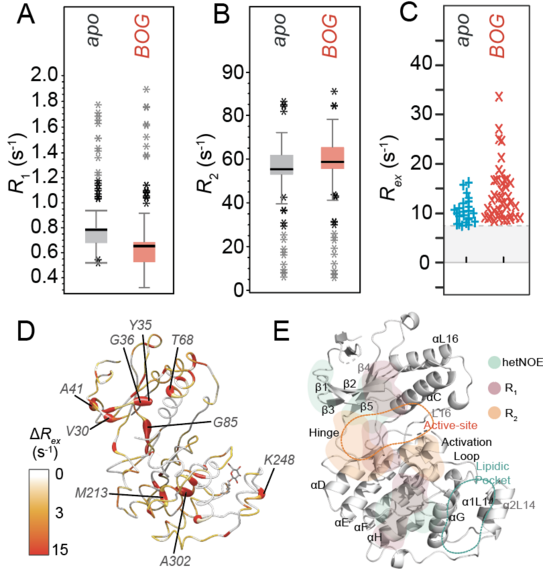
Mit dem Verorten einer weitreichenden allosterischen Interaktion zwischen der Lipidtasche und den für die Funktion und Regulation der Kinase eine Rolle spielenden Bereichen ist die Grundlage für weiterführende medizinische chemische Forschung in diesem Kontext gegeben. Können Liganden gefunden werden, die eine ausreichende Affinität und passende sterische Eigenschaften aufweisen, ist eine Modulation der Proteinfunktionalität, ob aktivierend oder inhibierend, sehr wahrscheinlich.
Lipid Pocket Binders Impose Allosteric Changes of Protein Dynamics Around the Active Site of the Protein Kinase p38α
S. M. Gómez, L. T. Homberg, M. Bührmann, D. Rauh, and R. Linser,
Angewandte Chemie International Edition. (2026): e22665.






