Präzise Abstandsmessung in DNA-G-Quadruplex-Paaren
- Neues aus der Fakultät 2020

Die DNA des Menschen liegt hautsächlich als verdrillter Doppelstrang vor, es gibt aber auch eine viersträngige Variante (sogenannte "G-Quadruplexe"), die sich aus Guanin-reichen Sequenzen zusammensetzt und einem säulenartigen Stapel gleicht. Für diese wurden in den letzten Jahren mehr und mehr biologische Funktionen und medizinische Relevanz entdeckt. Um die Rolle dieser G‑Quadruplexe im Körper zu verstehen, muss deren Aufbau und Struktur aufgeklärt werden. Dies ist eine herausfordernde Aufgabe, da diese speziellen DNA-Formen eine hohe strukturelle Diversität aufweisen. Sind räumlicher Aufbau und biologische Funktion solcher DNA-Varianten bekannt, können gezielt Moleküle entwickelt werden, die an diese G-Quadruplexe binden und deren Funktion beeinflussen. Da G-Quadruplexen eine entscheidende Rolle bei der Entstehung verschiedener Krebsarten, aber auch bei HIV und Malaria, zugeschrieben wird, haben DNA-bindende Moleküle das Potenzial als Wirkstoffe Einsatz in der Medizin zu finden.
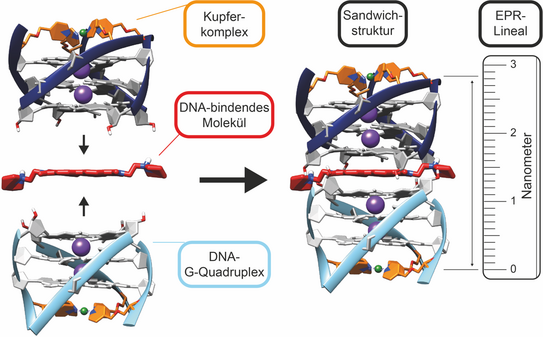
Bekannt ist zudem, dass G-Quadruplexe auch höhergeordnete Strukturen ausbilden können. Beispielsweise können sie sich paarweise zusammenlagern und sogenannte „Dimere“ bilden. Wenn sich kleine, üblicherweise flache Moleküle in dieses Dimer einlagern, spricht man von der Ausbildung von „Sandwich-Strukturen“. Der Nachweis und die räumliche Vermessung dieser Nanometer-großen Dimer- und Sandwichstrukturen ist schwierig. In enger Kooperation ist es nun den Dortmunder Gruppen um Jun.-Prof. Müge Kasanmascheff und Prof. Guido Clever gelungen, durch gezielten Einbau von Kupfer-Ionen in chemisch-modifizierte DNA-G-Quadruplexe eine Methode zu entwickeln, um solche Verbindungen in nie dagewesener Genauigkeit in Lösung zu vermessen. Dabei kam die EPR-Spektroskopie zum Einsatz, die den Abstand zwischen ungepaarten Elektronen der Kupfer-Ionen in den beiden Hälften des G-Quadruplex-Stapels messen kann. In Wasser eigentlich unlösliche, kleine Moleküle konnten dann in die gelösten G-Quadruplex-Dimere eingelagert werden, worauf hin sich der Abstand zwischen den Kupferkomplexen auf charakteristische Weise vergrößert. Dank der festen und starren Bindung der Kupferkomplexe in den G‑Quadruplexen konnten dabei bemerkenswert präzise Abstände bestimmt werden.
Die Arbeiten wurden im Rahmen des durch die Deutsche Forschungsgemeinschaft (DFG) geförderten Exzellenzclusters RESOLV durchgeführt und nun in einer als „Very Important Paper“ ausgezeichneten open access Publikation in der Fachzeitschrift Angewandte Chemie veröffentlicht. Die vorgestellte Methode eignet sich besonders zur genauen Strukturaufklärung dieser speziellen DNA-G-Quadruplexe und verspricht in Zukunft bei der Suche nach potenziell pharmakologisch wirksamen Substanzen helfen zu können.
Original Publikation:
“Precise Distance Measurements in DNA G‐Quadruplex Dimers and Sandwich Complexes by Pulsed Dipolar EPR Spectroscopy”
L. M. Stratmann, Y. Kutin, M. Kasanmascheff, G. H. Clever, Angew. Chem. Int. Ed. 2020, accepted, DOI: 10.1002/anie.202008618 (VIP Paper)
https://www.onlinelibrary.wiley.com/doi/10.1002/anie.202008618
Kontakt | Prof. Dr. Guido Clever Fakultät für Chemie und Chemische Biologie | JProf. Dr. Müge Kasanmascheff |
Tel. | +49 231 755 8677 | +49-231 755 3743 |
guido.clever@tu-dortmund.de | muege.kasanmascheff@tu-dortmund.de | |
Web | ||