Archiv 2023
Enzyme mit Nebenjob
- Neues aus der Fakultät 2023
Das kleine Protein Ubiquitin ist besonders dafür bekannt, andere Proteine für deren Abbau zu markieren, und wirkt dadurch in der Regulation aller zellulären Prozesse mit. Parallel zum Ubiquitin-System existieren verschiedene andere Ubiquitin-ähnliche Proteine, von denen Fubi trotz seiner immun-modulatorischen Aktivität nur wenig untersucht ist. Fubi wird von Zellen als Fusionsprotein mit dem ribosomalen Protein S30 hergestellt, und muss für funktionierende Ribosomen, den Proteinfabriken der Zelle, von S30 abgetrennt werden. Immunzellen nutzen dieses Nebenprodukt der Ribosom-Herstellung als Signalprotein, um beispielsweise in der Gebärmutter die Aktivität des mütterlichen Immunsystems lokal abzusenken und damit die Einnistung von Embryonen zu ermöglichen. Wie Fubi spezifisch von Proteasen erkannt wird und wie diese es von Ubiquitin unterscheiden war bisher nicht bekannt.
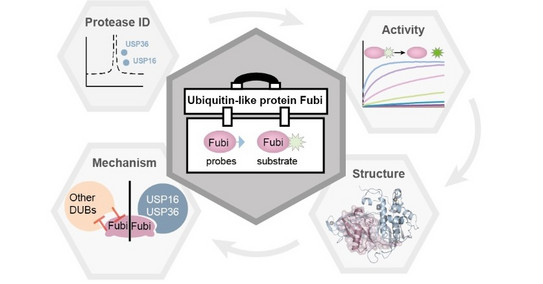
Wissenschaftler um Malte Gersch, Forschungsgruppenleiter am Chemical Genomics Center des Max-Planck-Instituts für molekulare Physiologie und der Fakultät für Chemie und Chemische Biologie der TU Dortmund, haben nun erste molekulare Einblicke in die Maschinerie gewonnen, die die Fubi-kontrollierte Reifung dieses Schlüsselproteins des Ribosoms ermöglicht. Mit Hilfe eines neu entwickelten chemischen Werkzeugkastens charakterisierten die Forscher auf molekularer Ebene, wie die zwei deubiquitinierenden Enzyme USP16 und USP36 über eine weitere spezifische Fubi-Protease-Aktivität verfügen. Diese doppelte Fubi/Ubiquitin-Spezifität erlaubt die Fubi-S30-Maturierung in zwei räumlich bestimmten Umgebungen der Zelle, und verhindert zugleich, dass die große Anzahl der weiteren nur Ubiquitin-spezifischen Enzyme Fubi prozessieren. Die Ergebnisse zeigen die molekulare Verschränkung des Ubiquitin-Systems mit dem bisher wenig erforschten Fubi-System, und werden zusammen mit dem entwickelten chemisch-biologischen Werkzeugkasten auch das Verständnis von Fubi als Protein-Modifikation in zellulären Prozessen erweitern.
Für diese Arbeit wurde Erstautorin Rachel O’Dea kürzlich in Wien mit einem Poster-Preis auf dem „Ubiquitin & Friends Symposium 2023“ ausgezeichnet.
Link zur Original-Veröffentlichung:
"Molecular basis for Ubiquitin/Fubi cross-reactivity in USP16 and USP36"
O’Dea R, Kazi N, Hoffmann-Benito A, Zhao Z, Recknagel S, Wendrich K, Janning P, Gersch M,
Nat Chem Biol, 2023